Gb, stop all'omeopatia da parte degli Mmg: è solo placebo
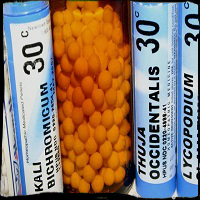
La sanità pubblica britannica spende 100mila euro l'anno
I farmaci omeopatici sono al massimo dei placebo, e non c'è nessun motivo per cui debbano essere rimborsati dalla sanità pubblica. Ad affermarlo è l'Nhs, la massima autorità britannica, che in una nuova linea guida in via di pubblicazione ha bocciato questo tipo di preparati. In un momento in cui i fondi scarseggiano, sottolineano gli esperti, meglio dirottare le risorse su rimedi di cui l'efficacia sia comprovata. La sanità pubblica, si legge nella linea guida, spende ogni anno circa 90mila sterline (100mila euro) per i farmaci omeopatici. "La modifica è stata proposta - spiega il direttore Simon Stevens, citato dal Guardian - perchè nel migliore dei casi l'omeopatia è un placebo e uno spreco degli scarsi fondi dell'Nhs, che potrebbero essere utilizzati meglio per trattamenti che funzionano".
Il documento prende di mira anche altre terapie finora rimborsate, dai trattamenti a base di erbe ai cerotti all alidocaina ai supplementi di omega-3, che verranno eliminati dal prontuario di quelli prescrivibili dai medici. Per quanto riguarda i farmaci omeopatici, il cui rimborso è stato più volte preso di mira da diversi esperti britannici, la linea guida li inserisce nel gruppo dei 'prodotti di bassa efficacia clinica, in cui c'è una mancanza di una evidenza chiara di utilità". Le parole degli esperti britannici sono molto simili a quelle utilizzate dalla Federal Trade Commission statunitense, che pochi mesi fa ha imposto ai produttori di scrivere chiaramente sulla confezione che non ci sono prove di efficacia.
pubblicità
"Per la maggior parte dei farmaci omeopatici - scrive l'ente Usa sul proprio sito - le prove di efficacia si basano solo su teorie tradizionali, e non ci sono studi validi che utilizzino il metodo scientifico. Pertanto le affermazioni per questi prodotti spesso possono confondere". In Europa solo Francia e Germania prevedono un rimborso parziale per i farmaci omeopatici, mentre in Italia è previsto solo da alcune iniziative locali, peraltro molto criticate, ad esempio in Toscana e nelle Marche. Nel nostro paese pochi giorni fa è scaduto il termine per la presentazione dei dossier all'Aifa per i preparati omeopatici, che secondo i produttori potranno quindi essere chiamati 'farmaci' come gli altri una volta ricevuta l'autorizzazione all'immissione in commercio da parte dell'agenzia. Per i dossier di prodotti già in uso non è però necessario fare i test clinici sull'uomo, che saranno invece indispensabili per registrare preparati futuri.
I Correlati
Il 57 per cento degli italiani ricorre all'omeopatia, 8 su 10 sono soddisfatti
L'Italia sulla fiducia è al 66%, subito dopo la Francia (73%), ma prima di Spagna (61%), Usa (60%) e Canada (50%)
Fofi: “Gli omeopatici non possono essere dispensati come medicinali terapeutici”
L’art. 85, comma 2, del citato D.Lgs. 219/2006 precisa che l’etichettatura e il foglio illustrativo dei medicinali omeopatici recano obbligatoriamente la frase “senza indicazioni terapeutiche approvate"
Cassazione: farmaci guasti anche per gli omeopatici
Secondo la Suprema Corte non è minimamente dubitabile la riconducibilità del farmaco omeopatico al concetto di medicinale, stante l’ampia definizione allo scopo fornita dal D.Lgs. n. 219 del 2006
E' guerra tra Burioni e Omeoimprese
L'Associazione diffida l'editore: l' 'Omeopatia è riconosciuta e tutelata'. Burioni: Il contratto che ho firmato con Rizzoli riporta un titolo completamente diverso
Ti potrebbero interessare
L'intelligenza artificiale può capire quando ridurre il carico di farmaci per gli anziani
Il chatbot generativo potrebbe migliorare i servizi di assistenza sanitaria geriatrica contribuendo al processo decisionale associato alla politerapia
Tumore del rene, immunoterapia aumenta l'aspettativa di vita
Pembrolizumab riduce la mortalità del 38% rispetto al placebo
Il 57% dei farmaci antitumorali approvati in via accelerata non dà alcun beneficio
Lo rivela uno studio pubblicato sul Journal of American Medical Association che sottolinea l'amara scoperta
Ema: Prove disponibili non supportano associazione causale tra agonisti del recettore GLP-1 e pensieri e azioni suicide e autolesionistiche
La revisione è iniziata nel luglio 2023, a seguito di segnalazioni di casi di pensieri suicidari e pensieri di autolesionismo da parte di persone che utilizzavano medicinali a base di liraglutide e semaglutide
Ultime News
Schillaci, sulla salute della donna impegnati per migliorare la prevenzione
Anche un sms per ricordare che possono accedere ad un controllo
Aifa, la carenza di ACE-inibitori in soluzione iniettabile in crisi renale sclerodermica (SRC) non dà rischi per i pazienti
I medicinali a base di enalapril iniettabile non sono disponibili in Italia da oltre vent’anni, in seguito alla revoca dell’Autorizzazione all’Immissione in Commercio (AIC) su rinuncia da parte dell’azienda farmaceutica titolare, nel 2000
Prescrizione degli accertamenti tributari e contributivi: la proroga Covid non ha effetto sugli anni successivi
La lettura combinata delle norme suggerisce, pertanto, di fare esclusivo riferimento ai termini di prescrizione e decadenza che scadono entro il 31 dicembre dell’anno in cui è disposta la sospensione degli adempimenti e dei versamenti tributari per e
I farmacisti puntano su prevenzione e digitale per promuovere salute e sostenibilità del servizio sanitario
Mandelli: "Un farmacista che rafforza il proprio ruolo qualificato di dispensatore del farmaco e sempre più presidio fondamentale per le attività di prevenzione e diagnosi precoce, a tutto vantaggio dei pazienti e della sostenibilità del Servizio San








Commenti