Un fattore di rischio genetico alla base della malattia di Crohn
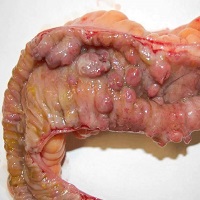
Le mutazioni del gene NOD2 sono fattori di rischio per la malattia di Crohn. Molti aspetti di come contribuiscono alla condizione sono sconosciuti
La malattia di Crohn, una malattia infiammatoria intestinale cronica, colpisce molte persone. Ad esempio, più dello 0,3% delle popolazioni del Canada e della Germania soffre della malattia e la sua incidenza è in aumento in tutto il mondo. Sono necessarie terapie migliori, ma i progressi nel trattamento della malattia di Crohn sono stati ostacolati dalla mancanza di comprensione di come si manifesti. Scrivendo in natura, Nayar fanno luce su un mistero di lunga data su un fattore di rischio per la malattia di Crohn e le loro scoperte hanno importanti implicazioni cliniche.
La malattia di Crohn può colpire qualsiasi parte dell'intestino.
pubblicità
Le variazioni genetiche, chiamate polimorfismi, del gene NOD2 sono la più forte associazione di rischio genetico per la malattia di Crohn; circa il 20% di tutto questo rischio di sviluppare la malattia è correlato a tre polimorfismi a singolo nucleotide di questo gene. Inoltre, le mutazioni NOD2 sono forti fattori predittivi per lo sviluppo di stenosi dell'ileo e per la necessità di un intervento chirurgico nella malattia di Crohn, che è un'associazione ampiamente convalidata tra le basi genetiche di questa condizione e le manifestazioni della malattia.
Tuttavia, il collegamento del gene NOD2 alla suscettibilità alla malattia ha presentato un paradosso. NOD2 è un recettore intracellulare (Fig. 1) che riconosce la molecola muramil dipeptide (MDP), un componente onnipresente delle pareti cellulari batteriche. Prima che NOD2 fosse descritto come un gene di rischio per la malattia di Crohn, la funzione di NOD2 era meglio compresa nelle cellule immunitarie che aiutano il ramo innato delle difese immunitarie. L'attivazione di NOD2 in queste cellule porta all'espressione di molecole infiammatorie chiamate citochine e una risposta infiammatoria anormalmente intensa può mediare il danno intestinale nella malattia di Crohn. Ci si sarebbe quindi potuti aspettare che NOD2mutazioni note come mutazioni con perdita di funzione, che non generano una versione completamente funzionale della proteina codificata, proteggono dalla malattia di Crohn. Tuttavia, tali mutazioni con perdita di funzione di NOD2 sono state identificate come fattori di rischio per la malattia. La ricerca successiva si è quindi concentrata su un aspetto diverso della biologia NOD2 nell'intestino, studiando come NOD2 funzionale mantiene l'omeostasi nell'intestino, dove la più grande biomassa del corpo di cellule immunologicamente attive è costantemente esposta a MDP dai microbi intestinali e come le mutazioni NOD2 perturbano questo equilibrio e portare alla malattia.
Il ruolo delle mutazioni NOD2 nell'emergenza della fibrosi dell'ileo era sconosciuto prima del presente studio. Gli autori hanno cercato di capire cosa guida l'infiammazione e la fibrosi nella malattia di Crohn e hanno collegato queste intuizioni biologiche a NOD2 attraverso la ricerca che utilizza cellule umane, tessuto intestinale umano e un modello di pesce zebra.
In primo luogo, gli autori hanno utilizzato il sequenziamento unicellulare dell'RNA dal tessuto infiammato di campioni di ileo rimosso durante l'intervento chirurgico da persone con malattia di Crohn. Queste cellule hanno rivelato una firma di espressione genica associata a macrofagi attivati e cellule di fibroblasti. Gli autori hanno anche identificato un tipo di cellula chiave che esprime marcatori di lignaggi cellulari sia mieloidi che fibroblasti. Queste scoperte suggeriscono che una popolazione di macrofagi infiammatori nell'ileo si differenzia per diventare fibroblasti attivati durante il decorso della malattia.
Sorprendentemente, gli autori dimostrano la conservazione evolutiva di queste popolazioni cellulari in un modello sperimentale di infiammazione intestinale - pesce zebra trattato con la molecola destrano solfato di sodio (DSS). Questa molecola è stata a lungo utilizzata per indurre danni intestinali e infiammazione in un modello di roditore standard. Il in vivola modellizzazione delle malattie infiammatorie intestinali umane è stata dominata dai modelli murini. Tuttavia, come dimostrano Nayar e colleghi, il pesce zebra offre un'utile alternativa per indagini ad alto rendimento e una rapida valutazione delle correlazioni con la malattia umana. In effetti, il pesce zebra e l'intestino dei mammiferi hanno una forma simile (morfologia). Inoltre, come gli esseri umani, il pesce zebra ha rami innati e adattivi delle loro risposte di difesa immunitaria e anche l'infiammazione intestinale del pesce zebra dipende dalla comunità di microrganismi intestinali. Gli strumenti di modifica genetica, come CRISPR, aiutano la rapida modifica dei geni di interesse per il pesce zebra.
Gli autori hanno studiato l'infiammazione intestinale nel pesce zebra progettato per avere un deficit di nod2 . Questi pesci, trattati con DSS, avevano un numero maggiore di cellule immunitarie leucocitarie nel loro intestino, un segno distintivo dell'infiammazione, rispetto al pesce zebra con nod2 normale . Ma il modello del pesce zebra è rilevante solo se è possibile stabilire una correlazione umana. Di conseguenza, utilizzando i dati di bambini con nuova diagnosi di malattia di Crohn, gli autori mostrano che un aumento del numero di copie di una mutazione NOD2 (associata al rischio di malattia di Crohn) era effettivamente correlato a una firma di espressione genica di macrofagi e fibroblasti attivati nell'ileo. tessuto.
Per comprendere la funzione NOD2 nelle cellule umane che possono differenziare in vitro , gli autori hanno utilizzato monociti del sangue periferico da volontari sani e hanno determinato se le cellule avevano una, due o nessuna copia delle mutazioni NOD2 legate alla suscettibilità alla malattia di Crohn. Le cellule sono state quindi differenziate in vitro con e senza MDP. Gli autori hanno osservato un numero maggiore di fibroblasti attivati per le cellule con due copie di mutazioni NOD2 rispetto alle cellule con NOD2 wild-type . Inoltre, un aumento del numero di NOD2le mutazioni erano associate a un corrispondente arricchimento nel numero di fibroblasti con una firma di espressione genica caratteristica delle cellule attivate. È interessante notare che il pesce zebra con deficienze nod2 , a cui è stato somministrato MDP, aveva una firma di espressione genica caratteristica dei fibroblasti attivati che persisteva anche durante il recupero da lesioni mediate da DSS, rispetto al pesce zebra che ha nod2 wild-type . Questi dati suggeriscono che i deficit di nod2 inibiscono il recupero (risoluzione) efficiente dalla fibrosi e dall'infiammazione.
Per chiarire ulteriormente le basi molecolari della firma di espressione genica legata alla fibrosi associata a NOD2mutazioni di rischio, gli autori hanno cercato regolatori trascrizionali a monte di questa via. Hanno identificato il gene che codifica per STAT3 come marcatamente sovraregolato nei fibroblasti e nei macrofagi attivati. STAT3 è un regolatore trascrizionale dei componenti chiave delle risposte infiammatorie e fibrotiche nelle malattie infiammatorie intestinali e agisce attraverso il recettore delle citochine gp130. Le analisi dei dati clinici hanno rivelato un'espressione sovraregolata dei geni regolati da gp130 che codificano per le proteine IL-6, oncostatina M e IL-11 nelle persone con malattia di Crohn che non hanno risposto alla terapia mirata alla proteina del fattore di necrosi tumorale (TNF) (anti-TNF gli anticorpi sono un trattamento comune per la malattia di Crohn). La scoperta supporta un ruolo per la segnalazione gp130 in questo gruppo di individui resistenti alla terapia.
Gli autori hanno ipotizzato che il blocco di gp130 potrebbe ridurre le anomalie che si verificano con la mutazione NOD2 . Hanno testato questa idea utilizzando bazedoxifene, un inibitore della gp130, su cellule umane trattate con MDP con mutazioni NOD2 . Il bazedoxifene ha infatti ridotto la firma di espressione genica associata al fibrotico e ha invertito i cambiamenti della forma cellulare che sono caratteristici dei fibroblasti attivati. Questo farmaco ha anche ridotto il danno intestinale riscontrato nel pesce zebra mutante nod2 trattato con DSS.
Partendo dalle caratteristiche cliniche della fibrosi nella malattia di Crohn, questo lavoro descrive un percorso molecolare legato alle mutazioni NOD2 associate alla malattia e si conclude con una potenziale intuizione terapeutica per affrontare i pressanti problemi clinici della fibrosi e della resistenza ai farmaci anti-TNF. Sostenendo la genetica e gli esiti clinici di questo percorso cellulare e molecolare, lo studio fornisce una road map per comprendere gli approcci terapeutici presenti e futuri.
Rimangono molte interessanti strade di indagine. NOD2 è l'unico percorso di riconoscimento descritto per MDP, ma questo documento dimostra i cambiamenti cellulari e molecolari indotti da MDP in assenza di nod2 in zebrafish. Ciò implica che ci sono percorsi di segnalazione MDP che non sono stati ancora descritti. Il bazedoxifene è stato inizialmente caratterizzato come un inibitore selettivo del recettore degli estrogeni, sollevando la preoccupazione che il farmaco possa avere effetti negativi su altre vie di segnalazione se usato come terapia per il morbo di Crohn. Il recettore gp130 ha più partner di legame del ligando che influenzano un'ampia gamma di risposte immunitarie. Quindi, la comprensione degli specifici ligandi di gp130 che orchestrano eventi molecolari mediati da NOD2 potrebbe portare a interventi terapeutici più selettivi, efficaci e più sicuri rispetto a quelli che inibirebbero globalmente la segnalazione di gp130 o prendere di mira altre vie di segnalazione clinicamente rilevanti, come gli enzimi Janus chinasi (inibitori per i quali sono in fase avanzata di sviluppo clinico per la malattia di Crohn).
Non tutti con la malattia di Crohn hanno mutazioni NOD2 associate al rischio di malattia. Infatti, in individui di determinati gruppi etnici, come le persone di origine cinese, malese o indiana, la malattia dell'ileo è una caratteristica clinica prominente della malattia di Crohn, tuttavia NOD2 non è associata al rischio di malattia in questa popolazione. Forse la firma molecolare dei macrofagi e dei fibroblasti attivati è la firma unificante rilevante per gli individui con malattia di Crohn dell'ileo. È probabile che diversi paesaggi genetici possano portare agli stessi risultati clinici e molecolari. Pertanto, i risultati di Nayar e colleghi spostano il campo un passo avanti verso una classificazione molecolare della malattia di Crohn che potrebbe chiarire una condizione complessa che ha circa 200 regioni genetiche associate al rischio di malattia e diverse manifestazioni cliniche.
fonte: Nature
I Correlati
Armuzzi: "In 20 anni cambio radicale nelle cure della malattia di Crohn e colite ulcerosa"
Gionchetti: "il sanguinamento è il sintomo più frequente della colite ulcerosa ma il sospetto di malattia si ha quando peggiorano i sintomi come la diarrea, il muco e il sangue"
Ecco il modello internazionale per la transizione dal paziente pediatrico all'età adulta
Romano (SIGENP): “Criteri fondamentali condivisi con l’universita del North Carolina, obiettivo accompagnare i giovani con esofagite eosinofila alla cura dopo i 18 anni”
Campagna mondiale per le patologie eosinofile, ESEO Italia illumina il Paese di magenta
Roberta Giodice: “Ringraziamo tutti i rappresentanti delle Istituzioni che hanno aderito con grande spirito di partecipazione alla campagna per le patologie eosinofile”
Medicina rigenerativa: una nuova potenziale terapia stimola la rigenerazione della mucosa intestinale in corso di infiammazione
. La scoperta apre la via ad una opzione terapeutica di grande rilevanza clinica. Il lavoro è stato pubblicato sul Journal of Clinical Investigation
Ti potrebbero interessare
Dal 17 settembre disponibile nelle farmacie lombarde il test per l'Helicobacter Pylori
Federfarma Lombardia insieme ad Alfasigma e Fondazione Poliambulanza per la prevenzione del tumore gastrico, che nel 2023 ha fatto registrare 15mila nuove diagnosi in Italia
Esofagite eosinofila, studio Sigenp definisce approccio e terapia
I risultati di una survey su scala nazionale saranno presentati al XXXI Congresso SIGENP (Società Italiana di Gastroenterologia, Epatologia e Nutrizione Pediatrica) a Palermo dal 26 al 28 settembre
Asse intestino-cervello, come il microbiota influenza le malattie
Minelli: "Organizzazioni microbiche intestinali disordinate sono state trovate in varie condizioni neuropsichiatriche come ad esempio depressione, ansia e disturbi"
Aumentano in Campania le malattie del fegato e dell’apparato digerente
Presso l’Azienda Ospedaliera Universitaria Luigi Vanvitelli nasce l’U.O.C. di Epatogastroenterologia









Commenti